静脉充血与血管瀑布:看懂这个公式是关键
静脉充血与血管瀑布现象
病理生理学重构、器官特异性机制与临床应用
重症医学

长期以来,重症监护医学的血流动力学管理主要由动脉侧模型主导,侧重于心输出量(CO)和平均动脉压(MAP)作为组织灌注的主要决定因素。然而,随着对静脉回流和微循环淤血认识的深入,特别是Castro等人(2025)在《Intensive Care Medicine Experimental》上发表的关于将静脉充血重构为动态Starling电阻现象的综述,以及近年来关于静脉过量超声评分(VExUS)的大量临床验证研究,我们正处于一个血流动力学范式转移的关键时刻。
本报告旨在结合Castro等人(2025)的最新理论框架及2024-2025年间的相关医学文献,对静脉充血和血管瀑布现象进行详尽的文献综述和深度分析。报告将深入探讨血管瀑布(Vascular Waterfall)的物理学原理及其在静脉系统的具体表现,剖析肝脏、肠道与肾脏在面对静脉高压时截然不同的耐受机制,揭示脓毒症血管麻痹状态下瀑布机制丧失的病理后果,并系统评估VExUS评分及多普勒波形分析在临床实践中的应用价值与局限性。通过将“液体反应性”与“液体耐受性”进行概念解耦,本报告为制定个体化、生理导向的重症治疗策略提供了坚实的理论基础。
第一章:血流动力学范式的演变与静脉系统的再认识
1.1 传统模型的局限性:从CVP到静脉回流
在一个多世纪的心血管生理学教学中,心脏的Starling曲线一直是液体管理的核心。这一模型暗示,只要心脏处于功能曲线的上升支,增加前负荷(通常以中心静脉压CVP为替代指标)就能通过Frank-Starling机制增加每搏输出量。这种观点将静脉系统简化为血液的被动储存库和回流导管,假定血流遵循简单的欧姆定律线性模型(Q = Delta P / R,即流量取决于平均体循环充盈压(Pmsf)与右房压(Pra)之差 。
然而,临床实践反复证明,单纯依赖CVP既不能准确预测液体反应性,也不能反映组织灌注的真实状态。更为严重的是,CVP的升高与器官功能衰竭,尤其是急性肾损伤(AKI)之间存在独立且显著的相关性 。这种相关性并非仅仅是因为心输出量下降(前向衰竭),更多是因为静脉高压导致的后向衰竭。
Castro等人(2025)的综述指出,生物体内的血管并非刚性管道,而是可塌陷的软管。当受到外部组织压力或平滑肌张力影响时,血流动力学行为不再遵循简单的线性压差关系,而是表现为“血管瀑布”或“Starling电阻”现象。这一视角的引入,解释了为何静脉充血并非均质的全身事件,而是具有高度器官特异性的病理过程。
1.2 血管瀑布现象的物理学定义
血管瀑布现象(Vascular Waterfall Phenomenon)描述了一种特殊的流体动力学状态:当血管内的压力低于某一临界值——即临界闭合压(Critical Closing Pressure, Pcrit)时,血流将不再取决于下游压力,而是由上游压力与Pcrit之间的压差决定 。
这一概念最早由Permutt和Riley在1963年提出,用于解释肺循环中的血流分布(即著名的West分区)。在West 2区,肺泡压超过肺静脉压但低于肺动脉压,此时血流由肺动脉压与肺泡压之差驱动,而与肺静脉压无关。这就好比河流流经瀑布,水流速度取决于河流上游的高度与瀑布边缘的高度差,而与瀑布下方水潭的水位无关——除非水潭水位上涨淹没了瀑布边缘。
Castro等人将这一概念从动脉和肺循环扩展至体循环静脉系统。他们提出,在肝脏、肠道等器官的静脉出口处,存在由组织压力或血管张力构成的Pcrit。当右房压Pra低于该Pcrit时,器官处于“保护”状态,中心静脉压的波动不会逆向传导至微循环;一旦Pra升高超过Pcrit,瀑布即被“淹没”,中心静脉压将直接作用于微循环,导致充血性损伤 。
1.3 Starling电阻与临界闭合压
Starling电阻(Starling Resistor)是实现血管瀑布效应的功能单元。它由Ernest Starling在早期实验中描述,指的是一种流体流经充满可变外部压力的腔室内的可塌陷管模型。
在静脉回流的生理学中,Starling电阻机制在两个层面发挥关键作用:
胸廓入口的大静脉: 在正常吸气过程中,胸内负压降低了右房压。理论上这应无限增加静脉回流,但实际上,当静脉进入胸廓时,血管壁因管内压低于大气压而塌陷,形成了一个限流点(Choke Point)。这使得静脉回流在Pra低于零时达到平台期,不再随Pra的进一步降低而增加 。
器官水平的微血管床: 這是Castro等人综述的核心。不同器官的静脉床具有不同的Pcrit。例如,腹腔内压(IAP)升高时,下腔静脉在穿过膈肌处可能形成Starling电阻;或者在肝血窦水平,库普弗细胞(Kupffer cells)的物理特性构成了对抗逆流的临界压力 。
第二章:血管瀑布的生理机制与争议
2.1 Guyton模型与血管瀑布的整合
Arthur Guyton的静脉回流曲线是理解循环生理的基石。Guyton提出,静脉回流(VR)由平均体循环充盈压Pmsf驱动,受静脉回流阻力Rvr阻碍,公式为:
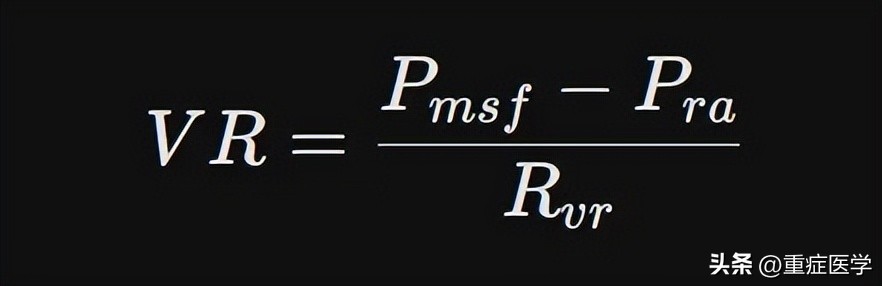
然而,这一公式仅在pra高于静脉塌陷压时成立。当Pra降低至大气压以下时,静脉回流曲线出现平台。这正是血管瀑布现象的体现。
最新的研究 指出,虽然Guyton模型在宏观上极其成功,但它将全身静脉床视为一个单一的集总参数(Lumped Parameter),忽略了各器官静脉床Pcrit的异质性。Castro等人(2025)的贡献在于将这一宏观模型细化,指出Pmsf并非直接驱动所有器官的回流,而是通过各器官局部的Pcrit进行调节。对于拥有有效血管瀑布的器官(如肝脏),驱动压是 Pmsf - Pcrit;而对于缺乏瀑布机制的器官(如肾脏),驱动压才是 Pmsf - Pra。
2.2 关于“瀑布”比喻的学术争议
尽管血管瀑布模型被广泛接受,但也存在学术争议。Badeer和Hicks等学者曾质疑“瀑布”这一比喻的准确性,认为流体动力学中的伯努利方程和泊肃叶定律足以解释可塌陷管流,无需引入“瀑布”这一可能引起误解的术语。他们指出,真实的瀑布涉及重力势能的转换,而血管内的现象更多是跨壁压(Transmural Pressure)导致的管腔几何形状改变。
然而,从临床教学和概念模型的角度来看,Castro等人坚持使用“血管瀑布”这一术语,因为它形象地捕捉了“下游压力去耦(Uncoupling)”这一核心特征 。在重症治疗中,理解这种去耦至关重要:它意味着在一定范围内降低CVP可能不会增加某些器官的血流(如果该器官处于瀑布状态),或者反之,CVP的升高在达到临界值前可能不会引起器官充血。
2.3 逆向血管瀑布(Reverse Vascular Waterfall)
Castro等人(2025)引入了一个引人注目的新概念——“逆向血管瀑布”。这并非指血液的持续倒流,而是指在无瓣膜的静脉床(如肝静脉)中,当下游压力(右房压)在心动周期的特定时相(如右房收缩或三尖瓣返流时)短暂超过上游压力时出现的脉冲式反流。
机制: 正常情况下,静脉系统的顺应性(Compliance)能够缓冲这种短暂的压力逆转。血管壁的塌陷或扩张形成了一个动态的阻力点,将这种反流限制在局部,形成短暂的涟漪而非洪流。
病理状态: 当静脉系统因容量过负荷而处于最大扩张状态(顺应性极低)时,这种缓冲机制失效。此时,右心房的压力波(如巨大的V波)将毫无阻碍地传导至实质器官。这种“逆向瀑布”的失守,是多普勒超声上观察到收缩期反流(Systolic Reversal)的病理生理基础 。
第三章:器官特异性血流动力学:缓冲与脆弱的二元对立
静脉充血的临床表现具有极大的异质性。为何有些心力衰竭患者即便CVP高达20 mmHg肝功能仍基本正常,而肾功能却迅速恶化?Castro等人(2025)提出的框架通过器官特异性的血管瀑布机制完美解释了这一现象。
3.1 肝脏:具备完善缓冲机制的器官
肝脏位于门静脉系统和下腔静脉之间,拥有独特的双重血供和复杂的微循环结构,使其对静脉高压具有较强的缓冲能力。
3.1.1 肝血窦的保护作用
肝血窦内皮细胞极其独特,它们具有筛板状结构且缺乏基底膜。Castro等人推测,肝血窦内皮细胞及库普弗细胞在面临压力升高时,可能会发生形态改变突入管腔,主动形成一个Pcrit,从而维持肝小叶内的压力相对稳定 。这构成了“肝脏血管瀑布”。只要下腔静脉压(IVC Pressure)低于这一临界值,肝脏的微循环灌注就不受下游压力波动的影响。
3.1.2 肝动脉缓冲反应(HABR)
当静脉充血导致门静脉有效灌注压下降时,肝脏启动肝动脉缓冲反应(Hepatic Arterial Buffer Response)。腺苷的局部积聚导致肝动脉扩张,增加动脉血流以补偿门静脉流的减少 。这种代谢性的调节机制为肝脏提供了第二层保护,维持了氧供。
3.1.3 顺应性与容量储备
肝脏本身是一个巨大的血液储存库,具有极高的血管顺应性。它可以像海绵一样扩张,容纳额外的血容量,从而在机械上缓冲逆向传导的压力波。
3.1.4 缓冲失效的后果
尽管有上述保护机制,当CVP持续显著升高并超过肝脏的Pcrit时,保护终将失效。
低氧性肝炎(Hypoxic Hepatitis): 淤血导致窦周水肿,增加了氧气从血液向肝细胞扩散的距离。
腹水形成: 高静水压迫使富含蛋白的淋巴液进入Disse间隙,当超过淋巴回流能力时,液体漏入腹腔 。
多普勒信号: 肝静脉多普勒波形从正常的三相波(S > D)变为S波减小,最终出现S波反转(Systolic Reversal)。这标志着“逆向瀑布”缓冲机制的崩溃,右房压力直接轰击肝实质 。
3.2 肠道:部分保护与高度敏感
肠道处于门静脉系统的上游。它受到门静脉压力的保护(门静脉压通常高于体循环静脉压),形成了一个天然的压力阶梯。然而,肠道微循环对淤血极为敏感。
3.2.1 门静脉瀑布
正常的门-体压力梯度充当了电阻。CVP的轻度升高首先被这一梯度吸收,不会立即影响肠道毛细血管压。Castro等人指出,肠道的血管瀑布效应部分来自于这种解剖学上的压力差 。
3.2.2 黏膜缺氧与屏障功能障碍
肠绒毛的逆流交换机制使其顶端处于相对缺氧状态。静脉淤血会迅速导致毛细血管滤过增加,引发黏膜水肿。这种水肿不仅增加了氧弥散距离,还可能压迫微血管,导致“充血性缺血”。肠道屏障功能的破坏可导致细菌移位,诱发全身炎症反应,这是右心衰竭合并脓毒症的重要机制之一。
3.2.3 腹腔内高压(IAH)的恶性循环
肠道水肿会导致腹腔内压(IAP)升高。IAP作为外部压力作用于下腔静脉和肾静脉,形成新的Starling电阻。这进一步阻碍了静脉回流,形成“充血-水肿-高压-更充血”的恶性循环 。
3.3 肾脏:缺乏保护的脆弱器官
与肝脏和肠道形成鲜明对比的是,肾脏被证实缺乏有效的静脉瀑布机制,这使其成为静脉充血最脆弱的受害者 。
3.3.1 直通式压力传导
肾静脉不仅无瓣膜,而且在解剖上缺乏类似的括约肌或特殊的窦状隙结构来缓冲压力。研究表明,下腔静脉压力的升高会以1:1的比例直接逆向传导至肾小管周围毛细血管网 。
3.3.2 充血性肾病(Congestive Nephropathy)的机制
肾脏被包裹在一个坚韧、无顺应性的被膜(肾囊)中。
间质压力升高: 静脉高压迅速导致肾间质水肿。由于肾囊限制了体积膨胀,肾间质静水压急剧上升。
肾小管压迫(Tubular Tamponade): 高间质压压迫肾小管,增加了小管内的静水压。
滤过梯度丧失: 肾小球滤过率(GFR)取决于跨肾小球压差(PGC - PBowman)。肾小管压力升高直接传递至鲍曼氏囊,抵消了滤过压。因此,即使肾动脉灌注压(MAP)保持不变,单纯的静脉压升高也足以导致GFR暴跌 。
3.3.3 肾脏多普勒特征
由于缺乏缓冲,肾内静脉血流对下游压力波动极其敏感。
正常: 连续性血流(类似静脉的“河流”)。
淤血进展: 随着肾间质压力升高,收缩期的高组织压开始阻断静脉流出,导致血流变为双相(Biphasic)。
严重淤血: 收缩期血流完全中断,仅在舒张期有血流(Monophasic/Diastolic-only)。这种“断流”现象(Discontinuous Flow)是肾脏血管瀑布缺失的直接证据——外部压力(间质压)周期性地超过了血管内压,完全阻断了血流。
第四章:病理生理学场景:从心力衰竭到脓毒症
4.1 心力衰竭:典型的后向衰竭
在心力衰竭中,主要的病理机制是容量过负荷导致Pmsf和Pra同时升高,淹没了各器官的血管瀑布。此时,器官保护机制失效,全身进入静脉高压状态。这是VExUS评分应用最成熟的领域。
4.2 脓毒症与血管麻痹:瀑布的消失
将血管瀑布理论应用于脓毒症(Sepsis)揭示了一个更为复杂的图景。脓毒症不仅是分布性休克,更是血管张力调节的全面崩溃。
4.2.1 临界闭合压Pcrit的降低
在健康状态下,血管平滑肌张力维持着较高的Pcrit,保证了微循环的压力梯度。在脓毒症中,内毒素和炎性细胞因子(如过量的NO)导致平滑肌瘫痪(血管麻痹,Vasoplegia)。
后果: Pcrit急剧下降,接近Pmsf。这意味着血管瀑布消失了。
血流动力学影响: 循环系统变得“压力被动”(Pressure-passive)。组织灌注不再由精细调节的MAP - Pcrit决定,而是完全依赖于宏观的MAP - CVP压差。这解释了为何脓毒症患者对低血压如此不耐受——他们失去了维持微循环压力的“刹车”机制 。
4.2.2 液体复苏的陷阱
在血管麻痹状态下,液体复苏是一把双刃剑。
传统观点: 补充血容量以提高Pmsf,驱动静脉回流。
瀑布视角: 由于Pcrit极低,给予的液体会迅速平衡整个静脉系统的压力。CVP的升高不再被器官局部的瀑布阻挡,而是直接传递至毛细血管。由于内皮糖萼受损(毛细血管渗漏),这种压力的传导导致组织水肿的速度远快于非脓毒症患者。这就是所谓的“液体毒性”(Fluid Toxicity)在脓毒症中的机制基础 。
4.2.3 去甲肾上腺素的复位作用
Pinsky等人的研究指出,去甲肾上腺素不仅是升压药,它还能恢复血管张力,即提高Pcrit。
重建瀑布: 通过恢复血管张力,去甲肾上腺素重建了血管瀑布,恢复了器官的保护性压力梯度。
容量动员: 它收缩静脉,将非应力容量(Unstressed Volume)转化为应力容量(Stressed Volume),从而在不增加外部液体负荷的情况下提高Pmsf。因此,在血管麻痹性休克中,早期使用血管加压药在生理学上优于单纯的大量液体复苏。
第五章:诊断工具:VExUS评分与多普勒波形分析
理论的进步催生了新的诊断工具。VExUS(Venous Excess Ultrasound)评分系统正是基于上述生理学原理,旨在量化器官水平的静脉充血程度。


5.2 临床验证研究与证据
5.2.1 预测急性肾损伤 (AKI)
心脏外科: Beaubien-Souligny等人的开创性研究及后续验证()表明,VExUS Grade 3与心脏术后AKI密切相关(OR值可达3.86)。这是因为此类患者主要表现为右心功能不全导致的静脉高压,符合经典的充血模型。
一般ICU与脓毒症: Andrei等人(2023)的多中心研究 发现,在一般ICU人群中,VExUS预测AKI的能力不如心脏外科患者强。
原因分析: 脓毒症患者的AKI机制复杂,涉及炎症、微循环血栓和低灌注,不仅仅是静脉充血。此外,如前所述,脓毒症时的血管麻痹可能导致即使CVP不高,微循环也已受损;或者反之,CVP升高但由于缺乏张力,并未形成典型的搏动性波形传递。
5.2.2 肾静脉停滞指数 (RVSI)
Husain-Syed等人(2019)提出了RVSI,即心动周期中肾静脉无血流的时间比例。研究发现,RVSI与AKI的发生呈线性正相关,且比单纯的阻力指数(RI)更敏感 。在心衰治疗中,RVSI的改善(从断续流恢复为连续流)是肾功能恢复的强预测因子 。
5.2.3 门静脉搏动的预后价值
多项研究 指出,门静脉搏动分数(Pulsatility Fraction)> 50% 是预后不良的独立标志。在充血性心衰患者出院时,若仍存在严重的门静脉搏动,其再入院率和死亡率显著增加。这表明肝脏/肠道水平的残余充血是临床隐匿但病理危害巨大的状态。
5.3 局限性与伪影
VExUS并非完美。
肝硬化: 肝实质硬化会改变波形传递,可能导致在无全身充血时出现门静脉平坦或异常。
高动力状态: 年轻健康的运动员或高动力性休克患者,可能因右心室收缩有力而出现短暂的波形改变,需结合IVC直径排除 。
技术门槛: 肾静脉多普勒采集难度大,受呼吸和体位影响明显。
第六章:临床应用与治疗策略:从液体反应性到液体耐受性
Castro等人(2025)的综述不仅是理论更新,更直接指导临床决策,特别是提出了将“液体反应性”(Fluid Responsiveness)与“液体耐受性”(Fluid Tolerance)分离的重要性。
6.1 液体管理的双轨评估
传统的液体复苏策略遵循“只要有反应就给液”。然而,瀑布理论告诉我们:
液体反应性: 反映心脏处于Starling曲线的上升支,给液能增加CO。
液体耐受性: 反映器官静脉瀑布的状态,给液是否会导致微循环充血。
冲突场景: 一个脓毒症合并AKI的患者,可能仍有液体反应性(给液后CO增加15%),但已无液体耐受性(VExUS显示肾静脉断续流)。此时,继续给液虽然能提升CO,但增加的CVP会直接传导至无保护的肾脏,加重肾小管压迫,导致GFR进一步恶化。
推荐策略: 液体复苏的终点不应仅仅是液体反应性的消失,而应是液体耐受性边界的到达。当出现VExUS Grade 2或肾静脉波形改变时,应停止液体复苏,即使患者仍有容量反应性 。
6.2 PEEP的滴定策略
机械通气是医源性静脉充血的常见原因。PEEP通过增加胸内压,不仅影响静脉回流,还可能建立一个人为的“胸部血管瀑布”。
策略: 在滴定PEEP时,不仅要看氧合和肺顺应性,还要监测腹部静脉波形。如果提高PEEP导致门静脉出现搏动或肝静脉S波反转,说明PEEP已过度阻碍静脉回流,导致腹腔器官充血。此时应权衡肺复张的收益与腹部器官损伤的风险 。
6.3 去复苏(De-resuscitation)与利尿
对于已经出现明显VExUS异常的患者,积极的去复苏是必要的。
指导利尿: 利用VExUS评分指导利尿剂的使用比单纯依靠体重或出入量更精准。目标是将门静脉搏动指数降至
第七章:未来方向与研究空白
尽管血管瀑布理论为重症血流动力学提供了强有力的框架,但仍有诸多领域亟待探索:
脓毒症表型的细分: 未来的研究需要区分“充血主导型”和“血管麻痹主导型”脓毒症。VExUS在这两类患者中的指导意义可能截然不同。
自动化监测: 目前VExUS依赖操作者经验。开发能自动识别波形并计算RVSI或门静脉搏动指数的AI算法,是推广该技术的关键。
无创Pmsf与Pcrit测量: 虽然已有通过呼吸末屏气估算Pmsf的方法,但尚未广泛临床化。开发简便的床旁工具来实时监测这两个参数,将使我们能直接量化血管瀑布的跨压梯度。
微循环与大循环的耦合: 结合正交极化光谱成像(OPS)等微循环监测技术,进一步验证大血管(VExUS)充血与毛细血管水平淤血的时空关系。
结论
Castro等人(2025)关于静脉充血与血管瀑布现象的综述,标志着重症血流动力学从“流量中心”向“压力与流量并重”的回归,以及从“心脏中心”向“器官保护中心”的演进。核心结论如下:
静脉回流是动态的: 它受制于Starling电阻机制,Pcrit的存在使得血流与下游压力在一定范围内解耦。
器官是不平等的: 肝脏和肠道拥有天然的瀑布机制缓冲静脉高压,而肾脏缺乏此机制,是静脉充血的“哨兵”器官。
VExUS是新的听诊器: 它不仅诊断充血,更通过波形变化揭示了器官耐受机制崩溃的病理生理过程。
治疗需个体化: 在脓毒症和心衰管理中,必须将液体反应性与耐受性分离,利用血管活性药物恢复瀑布机制,并利用多普勒超声设定复苏的安全边界。
通过这一范式重构,临床医生可以更精准地解读CVP的升高,更理性地使用液体和利尿剂,从而在挽救生命的同时,最大程度地保护脆弱的终末器官。

