锰的4大用途:炼钢、电池、肥料、消毒,一文看懂
CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)
纯净的金属形态下,它的用途并不广泛。然而,它可以作为主要添加剂之一添加到钢中,使钢具有不锈钢的特性。因此,它的历史与铁的历史息息相关,即使它的化合物存在于洞穴壁画和古代玻璃中。
其化合物可用于电池、分析方法、催化剂、有机氧化物、肥料、玻璃和陶瓷染料、干燥机和营养补充剂,以满足我们身体对锰的生物需求。
此外,无论与无机物还是有机物(有机锰)相互作用,锰化合物都具有鲜艳的色彩。它们的颜色取决于氧化数或氧化态,其中+7是氧化剂和抗菌剂高锰酸钾(KMnO)中最具代表性的颜色。 4 .
除了之前在锰环境中的用途外,其纳米颗粒和金属有机骨架也是开发催化剂、吸附剂固体和电子设备材料的选择。
故事
锰的起源,与许多其他金属一样,与其最丰富的矿物有关;在这种情况下,软锰矿,MnO 2 因其颜色独特,且产于希腊马格尼西亚,人们将其命名为黑色镁砂。黑色甚至出现在法国的洞穴壁画中。
它最初的名字是锰,由Michele Mercati起,后来改为锰。MnO 2 还 是 铁通常用于使玻璃变色,根据一些研究,它还出现在斯巴达人的剑中,而在此之前,斯巴达人都是自己制造钢铁的。
锰因其化合物的颜色而受到人们的赞赏,但直到 1771 年,瑞士化学家卡尔威廉才提出它作为化学元素的存在。
后来,1774 年,Johan Gottlieb Gahn 成功还原 MnO 2 使用煤来生产金属锰;目前用铝还原或转化为硫酸盐 MgSO 4 ,最终发生电解。
19世纪,锰获得了巨大的商业价值,它证明了锰能够提高钢的强度,同时又不影响其延展性,从而产生了锰铁。同样,MnO 2 可用作锌碳电池和碱性电池的阴极材料。
属性出现
银色金属色。
原子量
54.938 u
原子序数 (Z)
25
熔点
1.246℃,
沸点
2.061℃,
密度
-室温下:7,21 g/mL。
– 熔点(液态):5,95 g/mL
熔化热
12,91千焦/摩尔
汽化热
221千焦/摩尔
摩尔热容
26,32焦耳/(摩尔·开尔文)
电负性
鲍林量表 1,55
电离能
第一级:717,3 kJ/mol。
二级:2.150 kJ/mol。
第三级:3.348 kJ/mol。
原子半径
127个经验小时
热导率
7,81瓦/(米XNUMX开尔文)
电阻率
1,44°C 时为 20 µΩ
磁序
顺磁性,对电场有较弱的吸引力。
硬度
莫氏硬度 6.0
化学反应
锰的电负性比元素周期表上与其最接近的元素相比要小,因此反应性较低。然而,在有氧气的情况下,它可以在空气中燃烧:
3锰(s)+2氧 2 (克)=> 锰 3 O 4 ()
它还可以在约 1.200°C 的温度下与氮反应形成氮化锰:
3锰(s)+氮 2 (s) => 锰 3 N 2
它也直接与硼、碳、硫、硅和磷结合;但不与氢结合。
锰易溶于酸,与锰离子形成盐(Mn 2+ )并释放氢气。它也能与卤素发生反应,但需要高温:
锰(硫)+溴 2 (克)=> 溴化锰 2 ()
有机复合材料
锰可以与碳原子形成键,Mn-C,从而形成一系列称为有机锰的有机化合物。
在有机锰中,相互作用是由于 Mn-C 或 Mn-X 键引起的,其中 X 是卤素,或者是由于正锰中心与芳香族化合物的共轭 π 系统的电子云的定位。
上述化合物的例子有苯基碘化锰、PhMnI、甲基环戊二烯基三羰基锰和(C 5 H 4 CH 3 )-Mn-(CO) 3 .
后者的有机锰酸盐与 CO 形成 Mn-C 键,但也与芳香环云 C 相互作用 5 H 4 CH 3 ,形成半三明治结构:
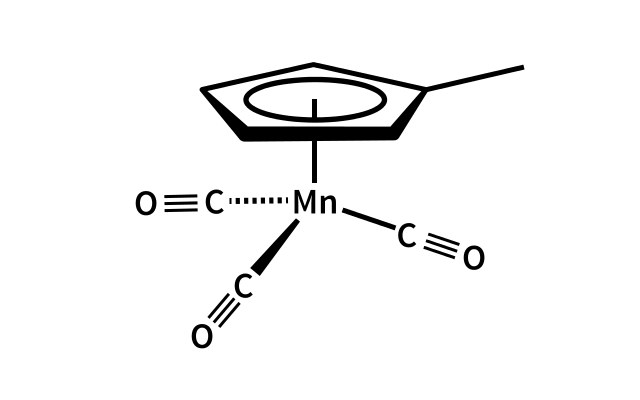
甲基环戊二烯基三羰基锰分子。来源:31Feesh 同位素
它有一个稳定的同位素 55 锰的丰度为100%。其他同位素均具有放射性: 51 锰, 52 锰, 53 锰, 54 锰, 56 Mn和 57 锰
电子结构和配置
锰在室温下的结构很复杂。虽然它被认为是体心立方(BCC)结构,但实验表明它的晶胞是一个扭曲的立方体。
第一种相,或称同素异形体(就金属作为化学元素而言),称为α-Mn,在725°C以下保持稳定;一旦达到该温度,就会转变为另一种同样“稀有”的同素异形体β-Mn。之后,β-Mn占据主导地位,直到1095°C,它再次转变为第三种同素异形体:γ-Mn。
相关: 摩尔溶液:概念、制备、示例
Γ-Mn 有两种可区分的晶体结构。一种是面心立方 (fcc),另一种是 面心四方 (fct)在室温下。最后,在1134°C时,γ-Mn转变为同素异形体δ-Mn,其结晶具有常见的体心立方结构。
因此,锰具有多达四种同素异形体,均与温度有关;至于与压力有关的形式,没有太多的参考书目可供参考。
在这些结构中,Mn 原子通过由其价电子控制的金属键连接,根据其电子排布:
3d 5 4s 2
氧化状态
锰的电子排布表明它有七个价电子;五个在3d轨道,两个在4s轨道。假设Mn阳离子存在,则在其化合物形成过程中,这些电子全部丢失。 7+ ,据说它的氧化数为+7或Mn(VII)。
高锰酸钾 4 (K + Mn 7+ O 2- 4 ) 是含有 Mn(VII) 的化合物的一个例子,它很容易通过其明亮的紫色来识别:

两种 KMnO4 溶液。一种是浓溶液(左),另一种是稀溶液(右)。图片来源:Pradana Aumars
锰可以逐渐失去每个电子。因此,它的氧化数也可以是+1、+2(Mn2 + ,最稳定的),+3(Mn3 + )等等,直到+7,前面已经提到过。
氧化数越高,它们获得电子的倾向就越强;也就是说,它们的氧化能力越强,因为它们会从其他物质中“窃取”电子来还原,从而满足电子需求。这就是为什么高锰酸钾 4 是一种强氧化剂。
颜色
所有锰化合物都具有颜色特征,这是由于dd电子跃迁所致,而dd电子跃迁会因氧化态和化学环境的不同而不同。因此,Mn(VII)化合物通常呈紫色,而Mn(VI)和Mn(V)化合物则分别呈绿色和蓝色。

绿色的锰酸钾溶液,K2MnO4。图片来源:Choij
公共领域
Mn(II)化合物看起来有些褪色,与KMnO形成对比 4 。例如,MnSO 4 和MnCl 2 呈固体状,淡粉色至近白色。
这种差异是由于 Mn 的稳定性 2+ ,其电子跃迁需要更多能量,因此几乎不吸收可见光辐射,而是几乎反射所有可见光辐射。
镁在哪里?

软锰矿是地壳中最丰富的锰元素来源。来源:Rob Lavinsky,iRocks.com – CC-BY-SA-3.0
CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)
锰占地壳的0,1%,在地壳元素中排名第十二。其主要矿床位于澳大利亚、南非、中国、加蓬和巴西。
主要锰矿物有:
-软锰矿(MnO 2 ) 含锰量 63%
-Ramsdelita(MnO 2 ) 含锰量 62%
-锰酸盐(Mn 2 O 3 .H 2 O),含62% Mn
-隐锰矿(KMn) 8 O 16 ) 含锰量 45 – 60%
-黑锰矿(Mn·Mn 2 O 4 ) 含锰量 72%
-褐铁矿(3Mn 2 O 3 硅锰 3 ) 含 50 – 60% Mn 和 (MnCO 3 ),含锰 48%。
只有锰含量超过 35% 的矿物才具有商业开采价值。
虽然海水中的锰含量极低(10 ppm),但海底大面积覆盖着锰结核,也称为多金属结核。这些结核含有锰簇以及一些铁、铝和硅。
据估计,结核中的锰储量远远大于地球表面的金属储量。
高品位结核含锰10%至20%,以及少量铜、钴和镍。然而,开采这些结核的商业盈利能力存在疑问。
含锰食物
锰是人类饮食中必不可少的元素,因为它参与骨组织的发育、形成以及形成软骨的蛋白聚糖的合成。
由于所有这些原因,充足的锰饮食是必要的,选择含有这种元素的食物。
以下是含锰食物列表,其数值以锰含量毫克/100克食物表示:
-菠萝 1,58 毫克/100克
-覆盆子和草莓 0,71 毫克/100 克
– 新鲜香蕉 0,27 毫克/100克
煮熟的菠菜 0,90 毫克/100克
红薯 0,45毫克/100克
– 大豆 0,5 毫克/100克
– 煮熟的卷心菜 0,22 毫克/100 克
-煮熟的西兰花 0,22 毫克/100 克
- 鹰嘴豆罐头 0,54 米 / 100 克
– 熟藜麦 0,61 毫克/100 克
– 全麦面粉 4,0 毫克/100克
– 煮熟的糙米 0,85 毫克/100 克
-所有品牌谷物 7,33 毫克/100 克
– 奇亚籽 2,33 毫克/100克
-烤杏仁 2,14 毫克/100克
通过这些食物,很容易满足锰的需求,经估算,男性需要摄入2,3毫克/天的锰;而女性需要摄入1,8毫克/天的锰。
生物学作用
锰参与碳水化合物、蛋白质和脂质的代谢,以及骨骼形成和对抗自由基的防御机制。
锰是多种酶活性的辅助因子,包括超氧化物还原酶、连接酶、水解酶、激酶和脱羧酶。锰缺乏与体重减轻、恶心、呕吐、皮炎、生长迟缓和骨骼异常有关。
锰参与光合作用,特别是参与光系统II的功能,光系统II参与水的分解形成氧气。光系统I和II之间的相互作用是ATP合成的必要条件。
锰被认为是植物固定硝酸盐所必需的元素,是氮的来源和植物的主要营养成分。
使用钢铁
锰本身的性能不足以满足工业应用的需求。然而,当锰以少量比例与铸铁混合时,就能形成钢。这种被称为锰铁的合金也被添加到其他钢材中,是使其具有不锈钢性能的关键成分。
除了提高强度和耐磨性外,它还能脱硫、脱氧和脱磷,去除钢铁生产过程中不需要的硫、氧和磷原子。所得材料强度极高,可用于制造铁轨、监狱笼栏、头盔、保险箱、车轮等。
锰还可以与铜、锌和镍形成合金,即生产有色合金。
铝罐
锰也用于生产铝合金,通常用于制造汽水罐或啤酒罐。这些铝锰合金具有耐腐蚀性。
化肥
锰如何像 MnO 一样对植物有益 2 或 MgSO 4、他 它被用于配制肥料,以便土壤富含这种金属。
氧化剂
Mn(VII),具体为 KMnO 4 是一种强氧化剂。它的作用是帮助水消毒,紫色的消失表明它已中和了水中的微生物。
它还可用作分析氧化还原反应中的滴定剂,例如用于测定亚铁、亚硫酸盐和过氧化氢。此外,它还是某些有机氧化反应的试剂,最常用于合成羧酸,包括苯甲酸。
由玻璃制成
玻璃天然呈现绿色,是因为其含有氧化铁或硅酸亚铁。如果添加一种能与铁发生反应并将其与玻璃分离的化合物,玻璃就会变色或失去其特有的绿色。
当锰以 MnO 形式添加时 2 出于这个目的,透明玻璃最终会呈现出粉红色、紫色或蓝色色调;这就是为什么总是添加其他金属离子来中和这种效果并保持玻璃无色(如果需要的话)。
另一方面,如果 MnO 过量 2 ,得到具有棕色或黑色色调的玻璃。
烘干机
锰盐,尤其是 MnO 2 ,Mn 2 O 3 , 二氧化锰 4 ,锰 2 O 4 (草酸盐)等用于在低温或高温下干燥亚麻籽油。
纳米粒子
与其他金属一样,它的晶体或聚集体可以小至纳米级;这些是锰纳米颗粒(Mn-NPs),专门用于非钢应用。
Mn-NPs在涉及金属锰的化学反应中表现出更高的反应性。虽然它们的合成方法较为绿色,但使用植物或微生物提取物,其潜在应用将更加环保。
它的一些用途是:
废水 - Depuran
– 满足锰的营养需求
– 用作抗菌剂和抗真菌剂
-降解染料
-它们是超级电容器和锂离子电池的一部分
-催化烯烃的环氧化反应
-纯化 DNA 提取物
在这些应用中,它们的氧化物纳米粒子(MnO NPs)也可以参与甚至取代金属粒子。
有机金属框架
锰离子可以与有机基质相互作用,形成金属有机骨架(MOF: 金属有机骨架 )。在这种类型的固体的孔隙或间隙中,由于具有明确的键和定向结构,化学反应可以以非均相方式产生和催化。
例如,来自 MnCl 2 4小时 2 O、苯三甲酸和二甲基甲酰胺,这些有机分子与Mn配位 2+ 形成MOF。
这种MOF-Mn能够催化烷烃和烯烃(例如环己烯、苯乙烯、环辛烯、金刚烷和乙苯)的氧化,将其转化为环氧物、醇或酮。氧化反应发生在固体及其复杂的晶体(或非晶态)晶格中。
参考文献M. Weld 等人(1920 年)。锰:用途、制备、开采成本及铁合金生产。检索自:digicoll.manoa.hawaii.eduWikipedia (2019). 锰 摘自:en.wikipedia.orgJ. Bradley 和 J. Thewlis。(1927)。α-锰的晶体结构。检索自:royalsocietypublishing.orgFullilove F. (2019)。锰:事实、用途和益处。研究摘自:study.com英国皇家化学学会。(2019)。元素周期表:锰。检索自:rsc.orgVahid H. 和 Nasser G. (2018). 锰纳米粒子的绿色合成:应用与未来展望——综述。《光化学与光生物学杂志B辑:生物学》第189卷,第234-243页。Clark J. (2017). 锰 摘自:chemguide.co.ukFarzaneh 和 L. Hamidipour。(2016)。锰金属有机骨架作为烷烃和烯烃氧化异相催化剂。《伊朗伊斯兰共和国科学杂志》27(1):31-37,德黑兰大学,ISSN 1016-1104。美国国家生物技术信息中心。(2019)。锰PubChem数据库。CID = 23930。检索自:pubchem.ncbi.nlm.nih.gov

